摘要
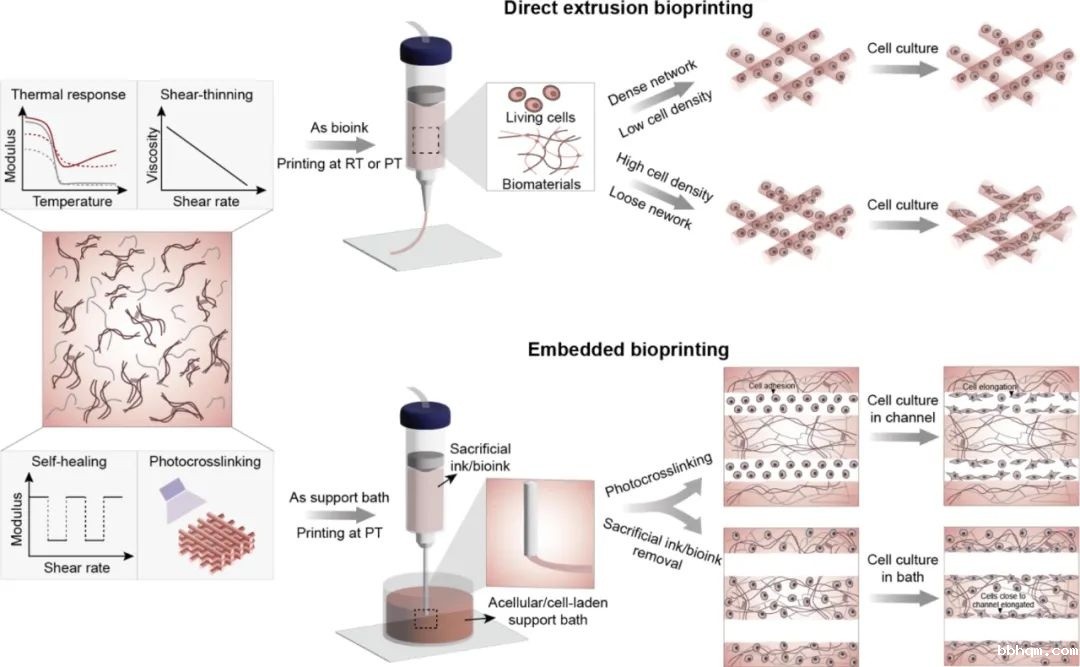
南洋理工大学研究团队开发了一种双重热响应和可光交联生物墨水,包括甲基丙烯酸明胶(GelMA)和甲基纤维素(MC)或甲基丙烯酸甲基纤维素(MCMA)。这种生物墨水既可用作直接挤出生物墨水,也可用作嵌入式生物打印的支撑槽,成功扩展了生理温度下直接和嵌入式生物打印能力。

研究背景
人体组织和器官是嵌入三维(3D)细胞外基质(ECM)中的各种细胞类型的分层复杂组装体。3D生物打印是一种生产载有3D细胞的结构的有前途的策略,能够制造与目标组织的天然生理学高度相似的仿生微环境生态位。生物打印窗口与可打印性和生物相容性之间的平衡有关。生物墨水的直接挤出打印并在永久交联之前同时保持良好的形状保真度并不是一项简单的任务。成功的生物墨水可打印性受多种因素控制,并与材料特性(例如流变学和凝胶化机制)和加工条件(例如温度)密切相关。
通常,较高的聚合物浓度和粘度可实现卓越的结构保真度,但会牺牲理想的泡孔行为。此外,在挤压过程中暴露于高剪切应力会导致细胞活力低下。提高温度可以降低许多生物墨水配方中的粘度,从而减少剪切应力并提高细胞活力,但通常会影响打印适性。相比之下,较低的温度可以通过增加粘度来帮助印刷适性。由于生物材料固有的特性和实验简单性,生物墨水通常在室温(RT)(20-25°C)而不是生理温度(PT)(37°C)下进行生物3D打印。然而,显著的温差和随后的剪切应力变化以及生物打印时间的延长可能导致细胞凋亡。
研究成果
南洋理工大学研究团队开发了一种双重热响应和可光交联生物墨水,包括甲基丙烯酸明胶(GelMA)和甲基纤维素(MC)或甲基丙烯酸甲基纤维素(MCMA)。这种生物墨水既可用作直接挤出生物墨水,也可用作嵌入式生物打印的支撑槽。
实验数据与分析
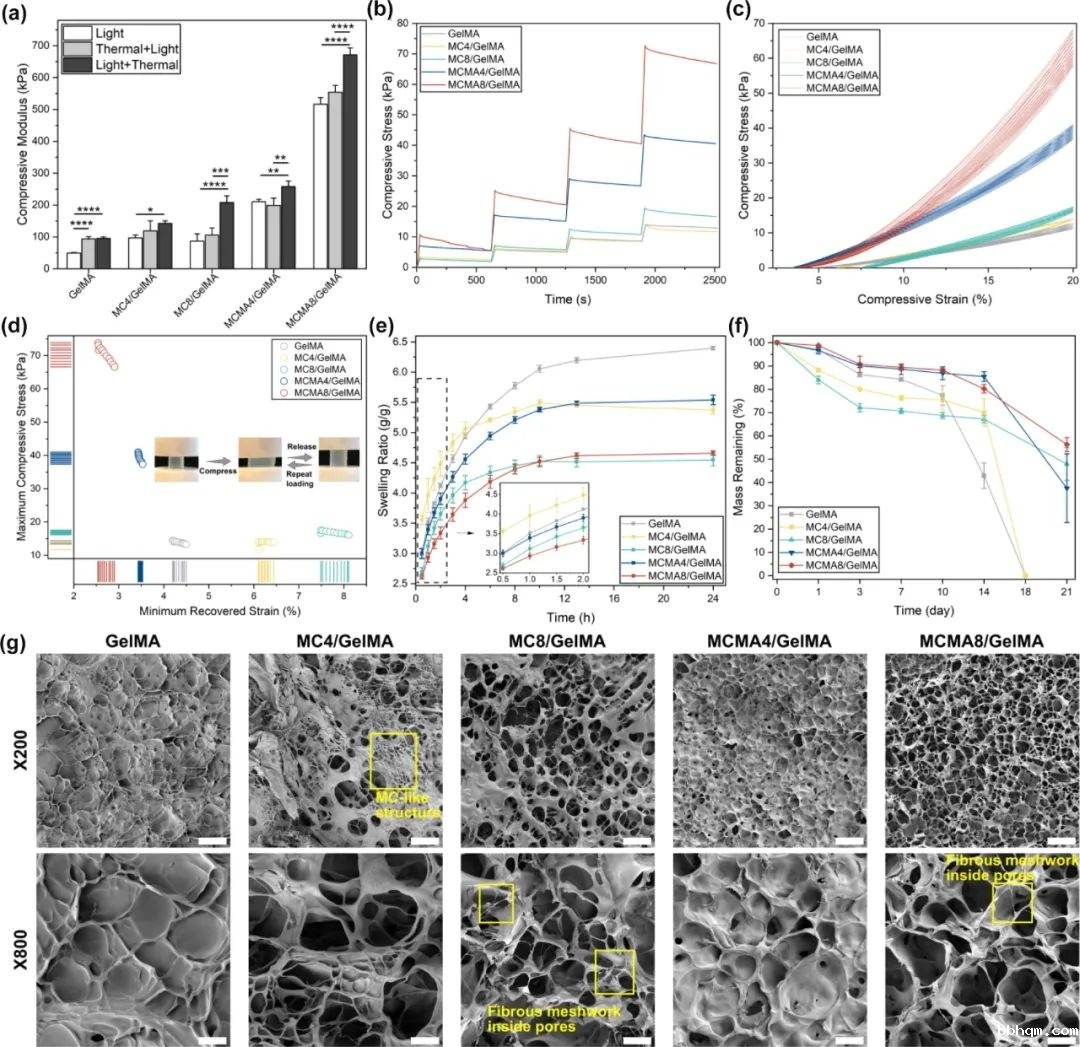
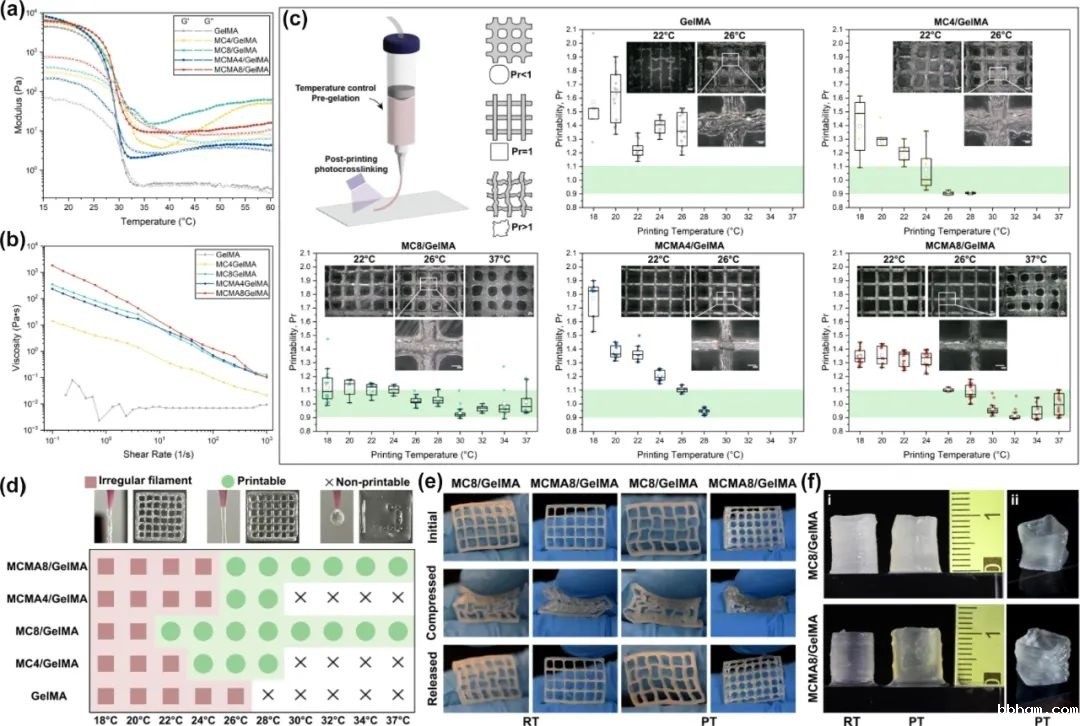
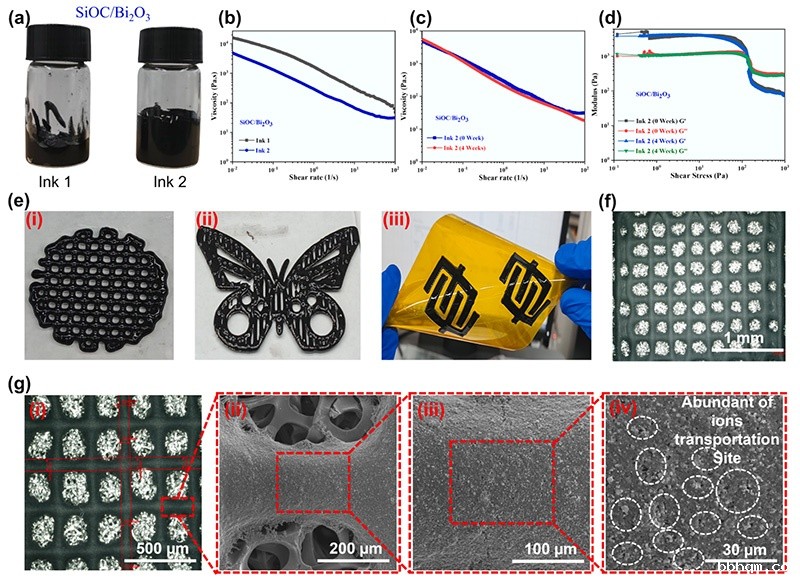
实验结果表明,通过调控GelMA与MC/MCMA的比例,可以精确控制生物墨水的流变学特性和交联行为。在生理温度下,该生物墨水表现出优异的剪切稀化特性和快速的自修复能力,能够在保持高细胞活力的同时实现复杂结构的精确打印。
光交联与热交联的协同作用不仅增强了水凝胶的力学性能,还提供了良好的生物相容性和可控的降解速率,为组织工程应用提供了理想的微环境。
嵌入式生物打印应用
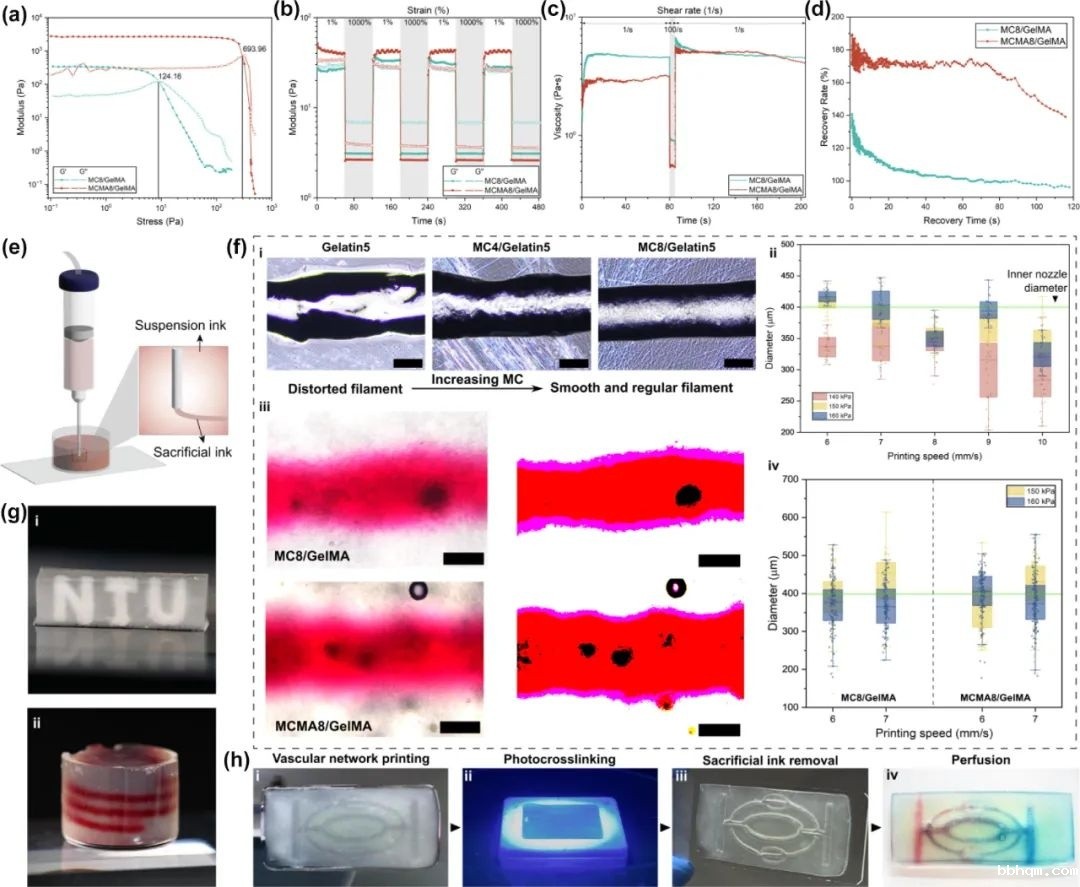
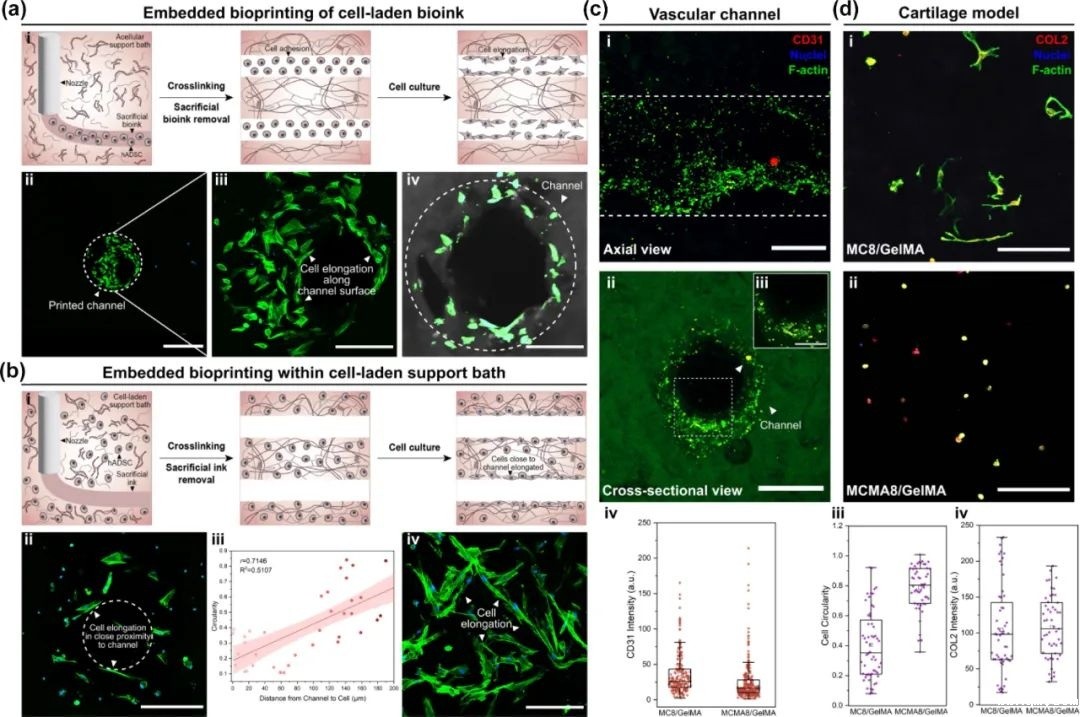
作为支撑浴,生物墨水可以通过嵌入式生物打印在PT制造复杂的载细胞结构,允许各种细胞类型和可灌注通道的空间模式,支撑浴充当基质以提供长期支持和细胞储存库。
通过这种方法,研究团队成功打印了具有复杂内部结构的组织模型,包括血管网络和多层细胞构建体,为药物筛选和疾病模型研究提供了有力工具。
结论与展望
基于GelMA、MC和MCMA开发的双重热响应和可光交联生物墨水,成功扩展了PT下直接和嵌入式生物打印能力。该生物墨水具有可调特性和自修复能力,支持复杂组织模型构建,为大规模组织工程应用提供了新途径。
这项研究不仅解决了传统生物打印中温度依赖性的挑战,还为开发更先进的生物墨水系统提供了理论基础和技术支持。未来的工作将集中在优化生物墨水配方以适应不同组织类型的需求,以及探索其在体内应用的潜力。